- ファンデルワールス力と水素結合
- 極性の有無と沸点
- 氷(水の結晶)
分子間力
分子間力
分子は共有結合によって形成されますが、分子同士は分子間力という力によって引き合っています。
分子間力:分子同士が引き合う力の総称、高校化学ではファンデルワールス力と水素結合のこと
分子間力の強さは、物質の沸点・融点を調べることで推測することができます。
ここからは、ファンデルワールス力と水素結合をそれぞれ見ていきましょう。
ファンデルワールス力
ファンデルワールス力は、すべての分子にはたらく引力です。
この引力の原因は、分子中の電子の動きにあります。
まず、前提として知っておいてほしいこととして、電子は原子核上を不規則に動いてます。(厳密には違いますが、高校化学ではこの考えでOKです。)
電子の位置はその瞬間によって異なるため、位置が偏ることがあります。
電子の位置の偏りから生じるのがファンデルワールス力です。
下のイラストは、水素分子を例にしたファンデルワールス力の原理図です。
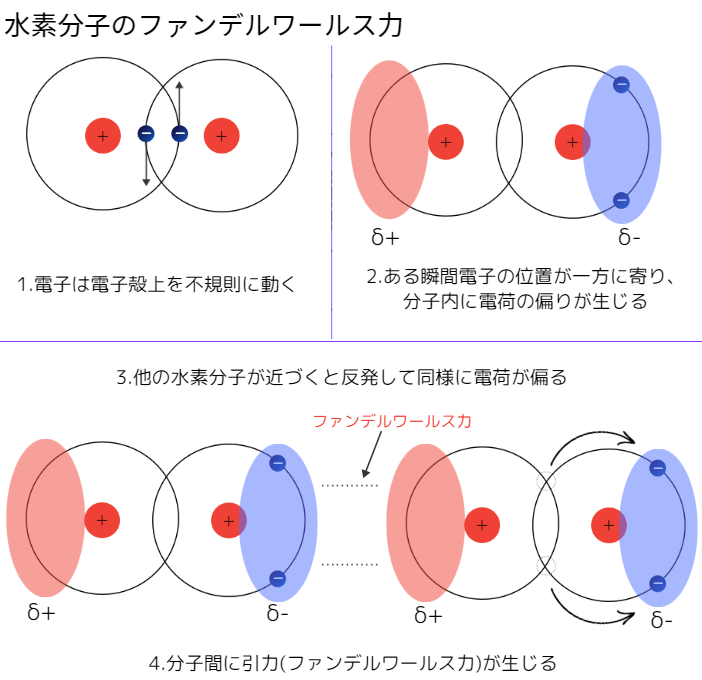
ファンデルワールス力はどんな分子にもはたらきますが、大小を決めるルールが3つあります。
- 分子量が大きいほど、ファンデルワールス力は大きい
→陽子・電子数が増えるため - 表面積が大きいほど、ファンデルワールス力は大きい
→力がはたらく場所が増えるため - 極性が大きいほど、ファンデルワールス力は大きい
→電荷の偏りが大きくなるため
極性分子間にはたらく静電気力
極性分子間では、ファンデルワールスに加えて静電気力がはたらくため結合が強くなります。
以下のグラフは極性分子(NH₃・H₂S・HCl)と無極性分子(CH₄・O₂・F₂)の沸点と分子量のグラフです。
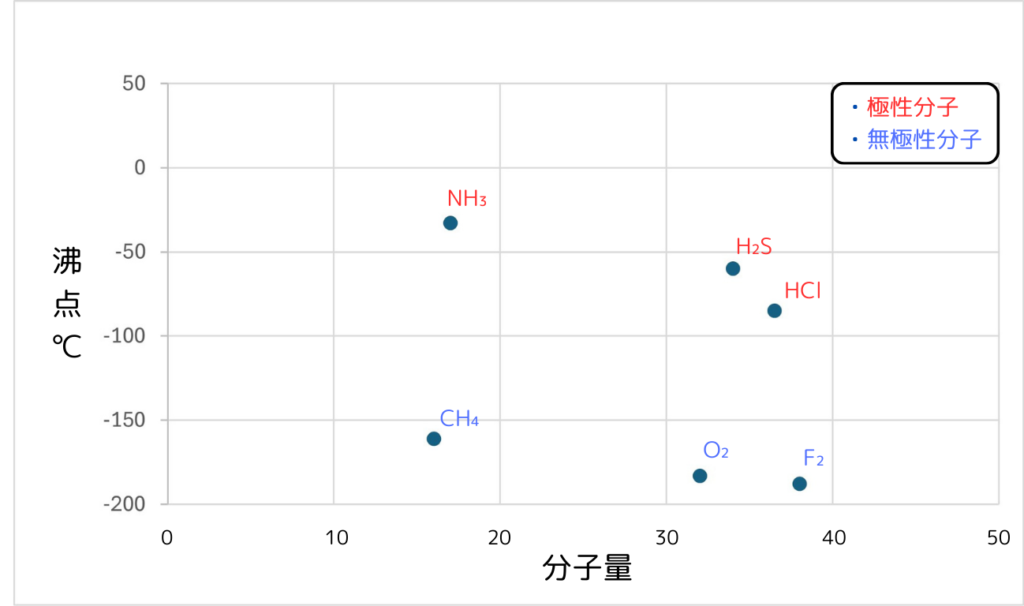
グラフから、無極性分子よりも極性分子の方が沸点が高いことがわかります。
水素結合
水素原子と電気陰性度の大きい原子とが結合している分子は、一般的な分子からなる物質よりも沸点・融点が高くなります。これは、水素結合と呼ばれる結合によるものです。
水素結合:窒素N・酸素O・フッ素Fの間に、水素をはさんでできる結合。(例:NH₃、H₂O、HFなど)
水分子H₂O間の水素結合を見てみましょう。
下図のように、水分子中の水素原子と、他の水分子中の酸素原子とが水素結合を作っています。
(実際は、1つの水分子は他4つの水分子と水素結合をしています。)
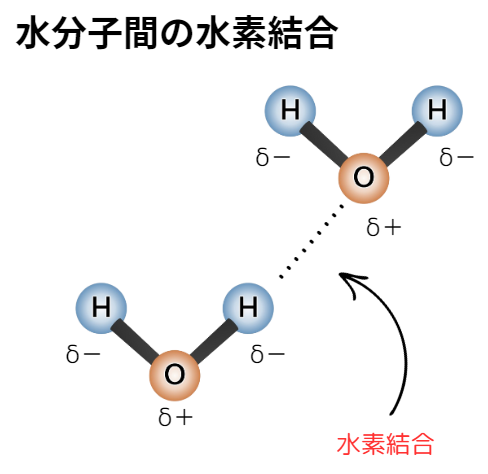
ファンデルワールス力と比べて電荷の偏りが大きいため、水素結合は、ファンデルワールス力よりも非常に強いです。
水素化合物の沸点
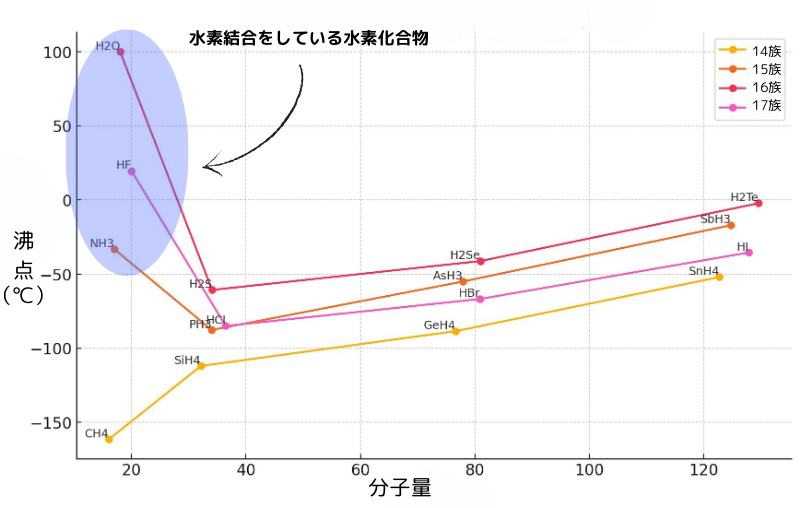
下のグラフを見ると、水素結合している物質が特別沸点が高い事が分かります。
また、分子量が増えると、沸点が上がっていることも分かります。
分子結晶
分子結晶と分子からなる物質の性質
分子からなる物質の結晶を分子結晶と呼びます。
- 分子間力が弱いため、融点・沸点が低くやわらかい
- 無極性分子からなる分子結晶は、昇華性を持つものがある…例:二酸化炭素・ナフタレン・ヨウ素など
- 結晶は電気を導かないが、HClのように水に溶かすと電離して電気を通すものがある。
氷(水)の構造
分子からなる水H₂Oは、他の物質からは見られない特異な性質を持ちます。
一般的に、物質は固体→液体→気体になるにつれて密度が小さくなっていきます。
しかし、H₂Oの密度は固体(氷)<液体(水)です。

その原因は、氷の構造にあります。
下のイラストは、氷と水の分子構造です。
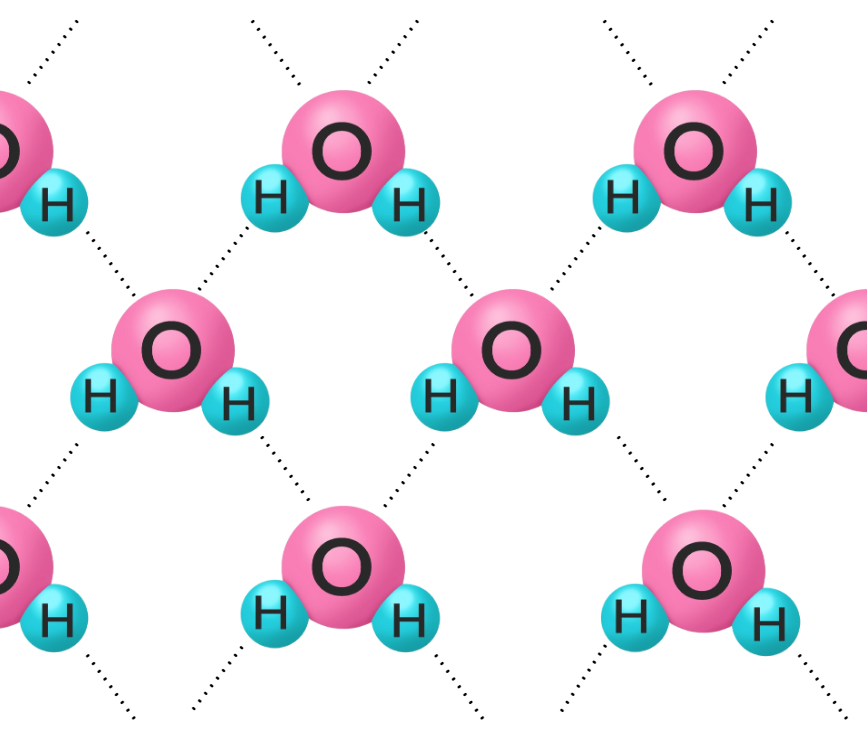
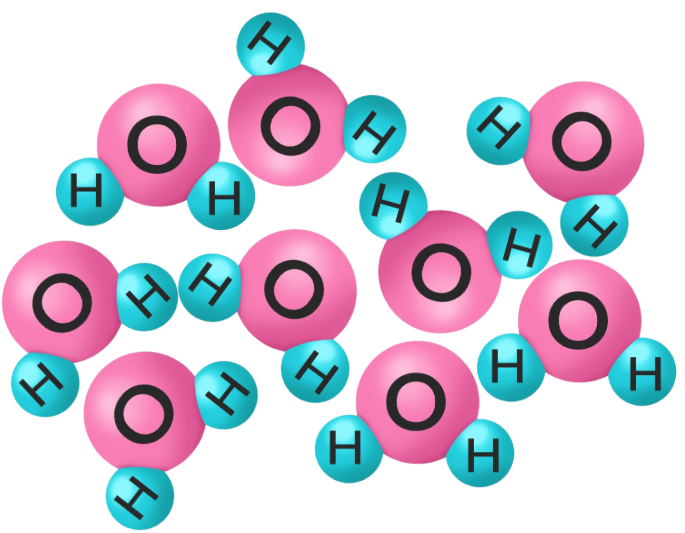
水は不規則に分子が集まっているのに対して、氷は分子が規則正しく配列し、隙間が多くなります。
そのため、同じ分子の数に対して氷の方が体積が大きい=密度が小さくなります。


