- 結晶格子・単位格子・配位数
- アモルファスと利用例
結晶
結晶格子と単位格子
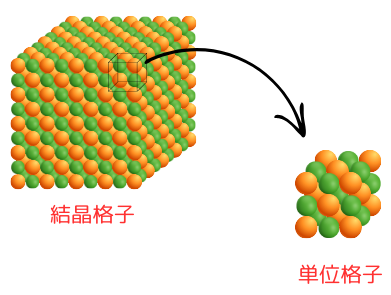
結晶とは、粒子が規則的に配列している固体のことでした。
この、粒子が規則的に配列している構造のことを結晶格子といいます。そして、結晶格子の最小のくり返し構造を単位格子といいます。
次回から、金属結晶・イオン結晶(+ダイヤモンド)の結晶格子・単位格子を解説していきます。
配位数
結晶格子中で、ある1個の粒子に隣接する他の粒子の数を配位数といいます。
例として、塩化セシウムのセシウムイオンの配位数を調べてみます。
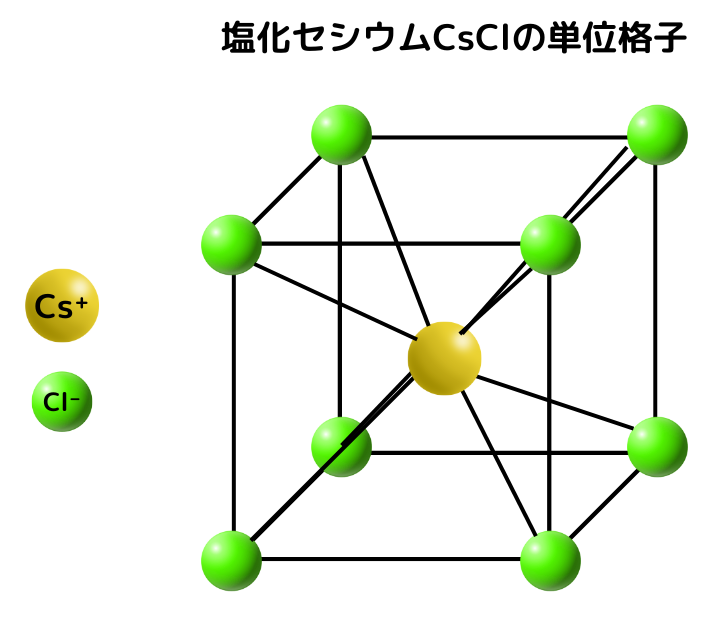
単位格子中の真ん中にあるセシウムイオンに着目すると、隣接しているのは角にある8つの塩化物イオンです。
よって、セシウムイオンの配位数=8となります。
もう1つ、次はアルミニウム(結晶)中のアルミニウム原子の配位数を調べてみます。
アルミニウムの単位格子は次のような構造を取っています。
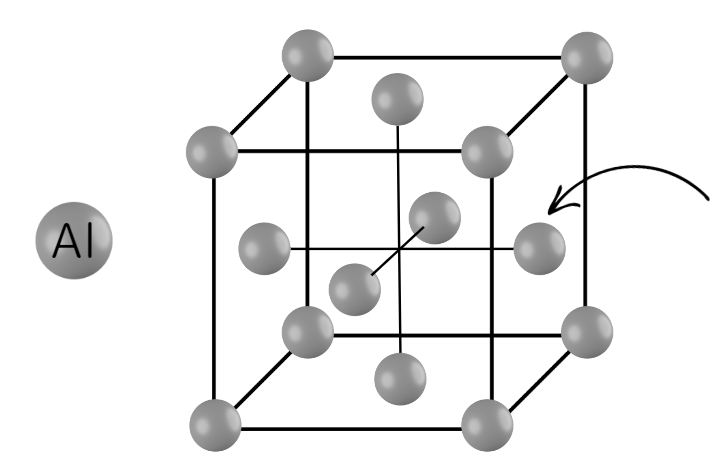
先ほどの塩化セシウムとは違い、中心に原子がないため数えづらいです。
そこで、矢印がついた右面中央の原子に着目し、更に右側にもう1つ単位格子をつなげると配位数が見えてきます。
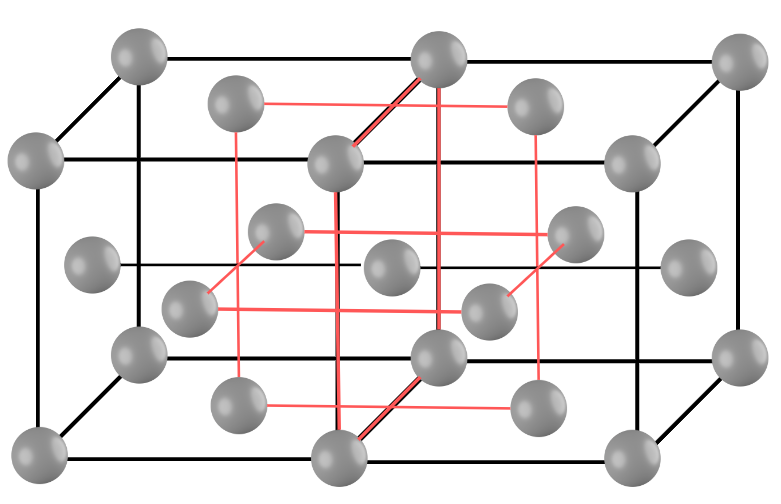
このようにつなげると、1つの原子の周りに隣接する原子は8つ(赤線を通る原子)であることがわかります。
よって、アルミニウム原子の配位数=12となります。
アモルファス
ほとんどの固体物質は結晶構造をもち、結晶質と呼ばれます。
しかし一部の固体物質には、粒子が不規則に配列し、結晶化していないものがあります。このような固体をアモルファス(または無定形)といいます。
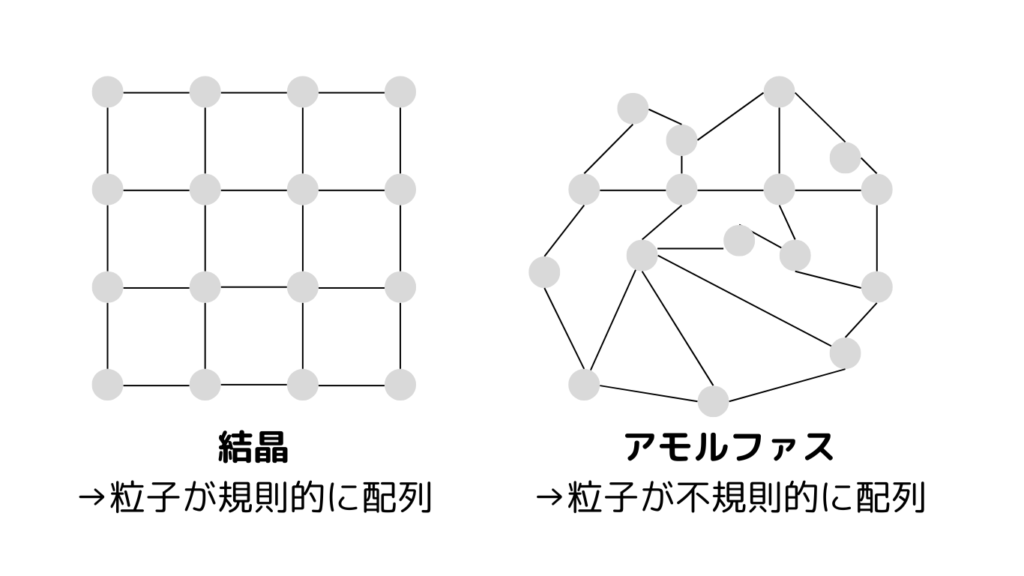
身近な例では、ガラス・ゴム・プラスチックなどがアモルファスに該当します。
※ここからの話は入試ではあまり問われませんので、特別覚えておく必要はありません。軽く知っておく程度で良いと思います。
アモルファスの生成
アモルファスは、高分子の液体を急速に冷却した際に作られます。
液体から固体になるとき、物質を構成する粒子は規則体な配列(結晶)を取ろうとします。
高分子の場合、ゆっくりと冷却しないと粒子が規則的に配列する前に粒子の位置が固定されてしまうため、アモルファスが生じます。
アモルファスの利用
アモルファスには、次のような性質があるため様々な用途に使用されています。
- 加工しやすい
- 安価で大量に製造できる
- 強靭で粘りがある
利用例を3つ挙げていきます。
アモルファス金属
一般的に金属は結晶ですが、高速で冷却することでアモルファス金属をつくることができます。
アモルファス金属には、強靭性・耐腐食性・磁気特性など通常の金属には見られない特異的な性質が見られます。
【利用例】:ノイズフィルタ・変圧器など
アモルファスシリコン
シリコンとはケイ素Si(Silicon)のことで、ケイ素原子が不規則な配列をとった固体をアモルファスシリコンといいます。
【利用例】:太陽電池・液晶パネルなど
ガラス
ガラスの主成分は二酸化ケイ素SiO₂です。二酸化ケイ素SiO₂は共有結合結晶として勉強しましたが、加工されてできるガラスはアモルファスに分類されます。
ガラスには様々な種類があり、光ファイバーなどの材料に用いられる石英ガラス、窓やコップに用いられるソーダ石灰ガラスなどがあります。(無機化学でもう少し詳しく勉強します。)


